Resumo das Características do Medicamento
1. NOME DO MEDICAMENTO VETERINÁRIO
Suprelorin 4,7 mg implante para cães e gatos
2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Substância ativa:
Deslorelina (sob a forma de acetato de deslorelina) 4,7 mg
Para a lista completa de excipientes, ver secção 6.1.
3. FORMA FARMACÊUTICA
Implante.
Implante cilíndrico branco a amarelo pálido.
4. INFORMAÇÕES CLÍNICAS
4.1 Espécie(s)-alvo
Cães, gatos (machos).
4.2 Indicações de utilização, especificando as espécies-alvo
Cães machos:
Para a indução da infertilidade temporária em cães machos saudáveis, não castrados, com maturidade sexual.
Cadelas na pré-puberdade:
Para a indução da infertilidade temporária para atrasar os primeiros sinais de estro e do cio e para prevenir a gestação numa idade jovem em cadelas não esterilizadas, saudáveis e sem maturidade sexual. O implante deve ser administrado entre as 12 e 16 semanas de idade.
Gatos machos:
Para a indução da infertilidade temporária e supressão do odor da urina e de comportamentos sexuais como libido, vocalização, marcação urinária e agressividade em gatos machos não castrados a partir dos 3 meses.
4.3 Contraindicações
Não existem.
4.4 Advertências especiais para cada espécie-alvo
Todas as espécies-alvo:
Nalguns casos, o animal tratado pode perder o implante. Se existirem suspeitas de falta da eficácia esperada, a presença subcutânea do implante deve ser verificada.
Cães machos:
A infertilidade é obtida a partir das 6 semanas até pelo menos 6 meses após o tratamento inicial. Os cães tratados devem, portanto, ser mantidos afastados de cadelas em cio nas primeiras 6 semanas após o tratamento inicial.
Durante os ensaios clínicos, um em cada 75 cães tratados com o medicamento veterinário acasalou e copulou uma cadela em cio no período de 6 meses após a implantação, não resultando, no entanto, em gestação. Se um cão tratado acasalar com uma cadela no período de 6 semanas a 6 meses após o tratamento, devem ser tomadas medidas apropriadas para excluir o risco de gestação.
Em casos raros foi referida uma presumível falta da eficácia esperada (na maior parte dos casos foi referida a falta de diminuição do tamanho testicular e/ou acasalamento). Apenas os níveis de testosterona (i.e., um marcador substituto estabelecido de fertilidade) podem definitivamente confirmar a falta de eficácia do tratamento.
Os acasalamentos que ocorram mais de 6 meses após a administração do medicamento veterinário podem resultar em gestação. Contudo, não é necessário manter as cadelas afastadas de cães tratados após as implantações subsequentes, desde que o medicamento veterinário seja administrado de 6 em 6 meses.
Em caso de presumível perda do primeiro implante, então a confirmação pode ser obtida através da observação da ausência de diminuição da circunferência escrotal, ou, através dos níveis de testosterona plasmática 6 semanas após a suposta data da perda, uma vez que, no caso de uma implantação correta é observada diminuição da circunferência escrotal e dos níveis de testosterona plasmática. Em caso de presumível perda do implante após reimplantação aos 6 meses, então é observado um aumento progressivo da circunferência escrotal e/ou dos níveis de testosterona plasmática. Em ambos os casos aconselha-se a administração de um implante de substituição.
Não se investigou a capacidade de procriação dos cães depois da normalização dos níveis de testosterona plasmática após a administração do medicamento veterinário.
Em relação aos níveis de testosterona (um marcador substituto estabelecido de fertilidade), durante os ensaios clínicos mais de 80 % dos cães a que se administrou um ou mais implantes voltou aos níveis normais de testosterona plasmática (≥ 0,4 ng/ml) no período de 12 meses após a implantação. Noventa e oito por cento dos cães voltou aos níveis normais de testosterona plasmática no período de 18 meses após a implantação. Contudo, os dados que demonstram a reversibilidade completa dos efeitos clínicos (redução do tamanho testicular, diminuição do volume de ejaculação, diminuição da contagem de espermatozoides e diminuição da libido), incluindo fertilidade após 6 meses ou implantação repetida, são limitados. Em casos muito raros a infertilidade temporária pode durar mais de 18 meses.
Durante os ensaios clínicos, a maior parte dos cães de pequeno porte (< 10 kg peso corporal) manteve níveis suprimidos de testosterona durante mais de 12 meses após a implantação. Para os cães de muito grande porte (> 40 kg peso corporal), os dados são limitados, mas a duração da supressão da testosterona foi comparável à observada em cães de médio e de grande porte. A utilização do medicamento veterinário em cães com menos de 10 kg ou com mais de 40 kg de peso corporal deve, portanto, ser sujeita a uma avaliação risco/benefício efetuada pelo médico veterinário.
A castração médica ou cirúrgica pode ter consequências inesperadas (i.e., aumento ou agravamento) no comportamento agressivo. Portanto, os cães com perturbações sociopáticas e exibindo episódios de agressões intraespecíficas (cão para cão) e/ou interespecíficas (cão para outra espécie) não devem ser castrados, nem cirurgicamente, nem com o implante.
Cadelas na pré-puberdade:
Durante os ensaios clínicos, o primeiro estro ocorreu 6 a 24 meses após a administração do medicamento veterinário em 98,2 % dos animais; para uma em cada 56 cadelas (1,8 %), a supressão do estro durou 5 meses. Especificamente, 44,6 % das cadelas apresentaram o primeiro estro entre 6 e 12 meses após a implantação, 53,6 % entre 12 e 24 meses após a implantação.
O medicamento veterinário só deve ser administrado a cadelas na pré-puberdade com idades entre as 12 e 16 semanas, que não apresentam sinais de estro. A medição dos níveis hormonais e os esfregaços vaginais podem ser utilizados para confirmar a ausência de estro.
Gatos machos:
Em gatos machos com maturidade, a indução da infertilidade e a supressão do odor da urina e dos comportamentos sexuais são obtidas, aproximadamente, a partir das 6 semanas até 12 meses após a implantação. Se um gato acasalar com uma gata antes das 6 semanas ou 12 meses após a implantação, devem ser tomadas medidas apropriadas para excluir o risco de gestação.
Quando implantado em gatos machos com 3 meses de idade, a supressão da fertilidade durou, pelo menos, 12 meses em 100 % dos gatos e mais de 16 meses em 20 % dos gatos.
Para a maioria dos gatos, no período de 2 semanas após a implantação, os níveis de testosterona diminuíram, seguidos da diminuição do volume testicular e da diminuição do tamanho das espículas penianas entre as semanas 4 e 8 após a implantação. Os comportamentos sexuais começam a diminuir no período de uma semana após o tratamento, começando com vocalização reduzida, seguida pela diminuição da libido, do odor da urina, da marcação urinária e da agressividade a partir de 4 semanas após a implantação. Alguns comportamentos sexuais, por exemplo, montar e morder o pescoço, também podem ter um componente social, no entanto, o gato com baixa de regulação não consegue completar o acasalamento ou induzir a ovulação da gata. Os efeitos clínicos sobre o odor da urina, a marcação urinária, o volume testicular, o tamanho da espícula peniana e os comportamentos sexuais começam a diminuir ao fim de aproximadamente 12 meses após a implantação.
O decurso temporal e a duração da baixa de regulação observada após o tratamento são variáveis, sendo 28 meses a duração máxima observada para a normalização da fertilidade após a implantação.
Num estudo de campo, 22 gatos machos receberam um segundo implante 12 meses após o primeiro, o que prolongou a duração da função reprodutiva e dos comportamentos sexuais suprimidos por mais um ano.
Em 1-3 % dos gatos machos, foi referida uma falta da eficácia esperada com base na expressão contínua de comportamentos sexuais, acasalamento resultante em gestação e/ou falta de supressão dos níveis de testosterona plasmática (um marcador substituto estabelecido de fertilidade). Em caso de dúvida, o proprietário do animal deve considerar manter o gato tratado separado de gatas quando a gestação for indesejável.
4.5 Precauções especiais de utilização
Precauções especiais para utilização em animais
Cães machos:
A administração do medicamento veterinário em cães machos na pré-puberdade não foi avaliada. Recomenda-se, portanto, deixar os cães machos atingir a puberdade antes de iniciar o tratamento com o medicamento veterinário.
Os dados demonstram que o tratamento com o medicamento veterinário diminuirá a libido do cão macho.
Cadelas na pré-puberdade:
Num estudo, das 34 cadelas que receberam o implante entre as 16 e 18 semanas de idade, um animal que recebeu o implante com 16 a 17 semanas de idade e dois animais que receberam o implante com 17 a 18 semanas de idade exibiram estro induzido pelo implante.
O tratamento repetido não foi avaliado em cadelas e, portanto, não é recomendado.
Após atingir a maturidade sexual depois de terminado o efeito de um implante, foram recolhidas informações sobre os ciclos de cio e a capacidade de procriação das cadelas: não foram observadas preocupações com a segurança reprodutiva. Num estudo de seguimento, seis gestações em cinco cadelas chegaram ao termo, com um a nove cachorros vivos. Devido à quantidade limitada de dados, a utilização em cadelas na pré-puberdade destinadas à reprodução deve ser feita de acordo com uma avaliação de benefício/risco pelo médico veterinário responsável.
A utilização em cadelas com maturidade sexual para suprimir a função reprodutiva e o ciclo do estro não é recomendada, devido ao risco de induzir um estro, o que pode causar patologia uterina e ovariana (metropatia, quistos) e gestação indesejada.
Gatos machos:
Não existem dados disponíveis para gatos com testículos retidos na altura da implantação. Recomenda-se esperar até que os testículos desçam antes de administrar o medicamento veterinário.
Existem dados limitados sobre o retorno à fertilidade normal após administrações repetidas do medicamento veterinário.
Não foi demonstrada a capacidade de procriação dos gatos depois da normalização dos níveis de testosterona plasmática após a administração do medicamento veterinário, especialmente em gatos na pré-puberdade. Por conseguinte, a decisão de utilizar o medicamento veterinário em gatos destinados à reprodução deve ser tomada caso a caso.
Precauções especiais a adotar pela pessoa que administra o medicamento veterinário aos animais
As mulheres grávidas não devem administrar o medicamento veterinário. Demonstrou-se que um outro análogo da GnRH é feto tóxico em animais de laboratório. Não foram realizados estudos específicos para avaliar o efeito da deslorelina quando administrada durante a gravidez.
Embora o contacto do medicamento veterinário com a pele seja improvável, lavar imediatamente a área exposta no caso de este contacto ocorrer, porque os análogos da GnRH podem ser absorvidos através da pele.
Ao administrar o medicamento veterinário, tome precauções para evitar a autoinjeção acidental, assegurando-se de que os animais estão bem presos e que a agulha de administração está protegida até ao momento da implantação.
Em caso de autoinjeção acidental, dirija-se imediatamente a um médico para que lhe seja removido o implante. Mostre o folheto informativo ou o rótulo ao médico.
4.6 Reações adversas (frequência e gravidade)
Todas as espécies-alvo:
A gonadectomia cirúrgica na pré-puberdade, bem como a supressão hormonal na pré-puberdade, podem atrasar o encerramento das fises em ossos longos, normalmente sem consequências clínicas ou patológicas.
Cão (macho e fêmea):
Durante os estudos de segurança/eficácia, foi observado frequentemente um inchaço moderado ou crosta no local do implante, durante 14 dias. Num ensaio de campo, foi referida frequentemente dermatite localizada com duração de até 6 meses.
Durante o período de tratamento, foram referidos efeitos clínicos raros:
Durante o período de tratamento, foram referidos raramente alterações da pelagem (por exemplo, perda de pelo, alopecia, alteração do pelo), incontinência urinária e sinais associados à baixa de regulação (por exemplo, diminuição do tamanho testicular, atividade reduzida, aumento de peso).
O testículo pode subir através do anel inguinal, em casos muito raros.
Foram referidos muito raramente um aumento transitório do interesse sexual, um aumento do tamanho testicular e dor testicular, imediatamente após a implantação. Estes sinais desapareceram sem tratamento.
Foram referidas muito raramente alterações comportamentais transitórias com o desenvolvimento de agressão (ver secção 4.4).
Em humanos e animais, as hormonas sexuais (testosterona e progesterona) modulam a suscetibilidade a convulsões. As convulsões epiléticas foram observadas muito raramente e foram notificadas em média 40 dias após a implantação, o tempo médio para o início dos sintomas foi de 14 dias após a implantação, no mínimo no mesmo dia da implantação, e de 36 semanas após a implantação, no máximo.
Gato:
Foram observadas frequentemente reações localizadas e transitórias, que consistiam em vermelhidão e dor ou calor, no dia da implantação. Num estudo de campo, foram observados frequentemente inchaços (< 5 mm) durante até 45 dias. Num estudo laboratorial, foram referidos inchaços graves (> 4 cm) com duração superior a 7 meses em 1 em cada 18 gatos.
Durante as primeiras semanas após a implantação, pode ser observado de forma transitória um aumento da atividade sexual e da deambulação em gatos machos com maturidade.
Sabe-se que o aumento da ingestão alimentar e o aumento de peso corporal é associado à esterilização. O peso corporal de alguns gatos tratados aumentou até 10 % durante o período de efeito.
A frequência dos eventos adversos é definida utilizando a seguinte convenção:
- muito frequente (mais de 1 animal apresentando evento(s) adverso(s) em 10 animais tratados)
- frequente (mais de 1 mas menos de 10 animais em 100 animais tratados)
- pouco frequente (mais de 1 mas menos de 10 animais em 1 000 animais tratados)
- rara (mais de 1 mas menos de 10 animais em 10 000 animais tratados)
- muito rara (menos de 1 animal em 10 000 animais tratados, incluindo notificações isoladas).
4.7 Utilização durante a gestação, a lactação e a postura de ovos
A segurança do medicamento veterinário não foi determinada durante a gestação e a lactação.
4.8 Interações medicamentosas e outras formas de interação
Desconhecidas.
4.9 Posologia e via de administração
Via subcutânea.
A dose recomendada é de um implante por cão ou gato, independentemente do seu tamanho (ver também ponto 4.4.).
A desinfeção do local de implantação deve ser efetuada antes da implantação para evitar a introdução de infeção. Se os pelos forem longos, devem ser bem cortados numa pequena área, se necessário.
O medicamento veterinário deve ser implantado por via subcutânea debaixo da pele laxa do dorso entre a parte inferior do pescoço e a região lombar. Evitar injetar o implante em tecido adiposo, dado que a libertação da substância ativa pode ser alterada em zonas pouco vascularizadas.
1. Retirar a tampa Luer Lock da seringa para implantes.
2. Prender o dispositivo de administração na seringa para implantes usando a conexão Luer Lock.
3. Levantar a pele laxa situada entre as omoplatas. Introduzir por via subcutânea todo o comprimento da agulha.
4. Premir completamente o êmbolo do dispositivo de administração e, ao mesmo tempo, retirar lentamente a agulha.
5. Exercer pressão na pele no local de inserção à medida que a agulha é retirada e manter a pressão durante 30 segundos.
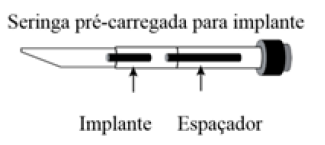
6. Examinar a seringa e a agulha para garantir que o implante não ficou na seringa ou na agulha e que o espaçador é visível. Pode ser possível palpar o implante in situ.
Repetir a administração de 6 em 6 meses para manter a eficácia em cães e de 12 em 12 meses para manter a eficácia em gatos.
Não administrar o medicamento veterinário se a bolsa de folha de alumínio estiver quebrada.
O implante é bio compatível e não necessita de ser removido. Contudo, se for necessário terminar o tratamento, o implante ou os seus fragmentos podem ser removidos cirurgicamente por um médico veterinário. Os implantes podem ser localizados através de ecografia.
4.10 Sobredosagem (Sintomas, procedimentos de emergência, antídotos), (se necessário)
Cão:
Não foram observadas reações adversas clínicas para além das descritas na secção 4.6 ou um nódulo junto ao local de injeção após a administração subcutânea simultânea de até 10 vezes a dose recomendada e até 15 implantes ao longo de um ano, ou seja, a administração simultânea de 5 implantes de 6 em 6 meses em 3 ciclos consecutivos ou a administração simultânea de 3 implantes de 3 em 3 meses em 5 ciclos consecutivos. Foram observadas convulsões num cão e numa cadela com 5 vezes a dose recomendada. As convulsões foram controladas com tratamento sintomático. No exame histológico foram observadas reações locais ligeiras com inflamação crónica do tecido conjuntivo e um certo grau de formação de uma cápsula e de deposição de colagénio, 3 meses após a administração subcutânea simultânea de até 10 vezes a dose recomendada.
Gato:
Num estudo laboratorial, onde gatos machos receberam 1 ou 3 implantes 3 vezes com intervalos de 6 meses, 3 em cada 8 desenvolveram um inchaço grave (> 4 cm) no local da injeção interescapular com duração de, pelo menos, 4 semanas após a 2.ª e/ou 3.ª implantação.
Foram referidos casos de infertilidade após a exposição a sobredosagem não contemplada na rotulagem em gatos recém-nascidos, bem como num gato com maturidade.
4.11 Intervalo(s) de segurança
Não aplicável.
5. PROPRIEDADES FARMACOLÓGICAS
Grupo farmacoterapêutico: Hormonas pituitárias e hipotalâmicas e análogos, hormonas libertadoras de gonadotrofinas (GnRH), código ATCvet: QH01CA93.
5.1 Propriedades farmacodinâmicas
O agonista da GnRH, a deslorelina, atua suprimindo a função do eixo hipófise-gónadas quando administrado numa dose baixa e contínua. Esta supressão resulta na incapacidade dos animais tratados, não castrados ou castrados cirurgicamente, de sintetizarem e/ou libertarem hormona estimuladora de folículos (FSH) e hormona luteinizante (LH), as hormonas responsáveis pela manutenção da fertilidade, bem como dos comportamentos sexuais secundários.
Em cães e gatos, a dose baixa contínua de deslorelina reduz a funcionalidade e o tamanho dos órgãos reprodutores masculinos, a libido e a espermatogénese e diminui os níveis de testosterona plasmática decorridas 4 a 6 semanas após a implantação. Pode observar-se um pequeno aumento transitório da testosterona plasmática imediatamente após a implantação. A determinação das concentrações plasmáticas de testosterona demonstrou o efeito farmacológico persistente da presença contínua de deslorelina na circulação durante, pelo menos, seis meses em cães e doze meses em gatos após a administração do medicamento veterinário.
Em cadelas sem maturidade sexual, a dose baixa contínua de deslorelina mantém os cães num estado de imaturidade fisiológica e previne o aumento dos níveis plasmáticos de estradiol e progesterona. Esta baixa de regulação hormonal suprime o desenvolvimento e a função dos órgãos reprodutivos femininos e sinais comportamentais de cio associados e alterações na citologia vaginal.
5.2 Informações farmacocinéticas
Cão:
Demonstrou-se que os níveis plasmáticos de deslorelina atingem um máximo 7 a 35 dias após a administração de um implante contendo 5 mg de deslorelina radiomarcada. A substância pode ser doseada diretamente no plasma até, aproximadamente 2,5 meses após a implantação. O metabolismo da deslorelina é rápido.
Gatos machos:
Num estudo que investigou a farmacocinética em gatos, foi demonstrado que as concentrações plasmáticas de deslorelina atingem um máximo em 2 horas (C max) a cerca de 100 ng/ml, seguido de uma diminuição rápida de 92 %, 24 horas após a implantação. Após 48 horas, observou-se uma diminuição lenta e contínua das concentrações plasmáticas de deslorelina. A duração da libertação de deslorelina dos implantes Suprelorin, calculada como concentrações plasmáticas de deslorelina mensuráveis, variou de 51 semanas a, pelo menos, 71 semanas (fim do estudo).
6. INFORMAÇÕES FARMACÊUTICAS
6.1 Lista de excipientes
Óleo de palma hidrogenado
Lecitina
Acetato de sódio anidro
6.2 Incompatibilidades principais
Desconhecidas.
6.3 Prazo de validade
Prazo de validade do medicamento veterinário tal como embalado para venda: 3 anos
6.4 Precauções especiais de conservação
Conservar no frigorífico (2 °C – 8 °C).
Não congelar.
6.5 Natureza e composição do acondicionamento primário
O implante é apresentado numa seringa para implantes pré-carregada. Cada seringa para implantes pré-carregada é acondicionada numa bolsa de folha de alumínio vedada, que é subsequentemente esterilizada.
Caixa de cartão contendo duas ou cinco seringas para implantes individualmente envolvidas por folha de alumínio que foram esterilizadas juntamente com um dispositivo de implantação (dispositivo de administração) que não é esterilizado. O dispositivo de administração é preso à seringa para implantes usando a conexão Luer Lock.
É possível que não sejam comercializadas todas as apresentações.
6.6 Precauções especiais para a eliminação de medicamentos veterinários não utilizados ou de desperdícios derivados da utilização desses medicamentos
O medicamento veterinário não utilizado ou os seus desperdícios devem ser eliminados de acordo com os requisitos nacionais. O dispositivo de administração pode ser reutilizado.
7. TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
VIRBAC 1ère avenue
2065 m LID
06516 Carros
FRANÇA
8. NÚMERO(S) DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
EU/2/07/072/001
9. DATA DA PRIMEIRA AUTORIZAÇÃO/RENOVAÇÃO DA AUTORIZAÇÃO
Data da primeira autorização: 10/07/2007
Data da última renovação: 17/05/2017
10. DATA DA REVISÃO DO TEXTO
Encontram-se disponíveis informações detalhadas sobre este medicamento veterinário no website da Agência Europeia do Medicamento http://www.ema.europa.eu/.
PROIBIÇÃO DE VENDA, FORNECIMENTO E/OU UTILIZAÇÃO
Não aplicável.
