Resumo das Características do Medicamento
NOME DO MEDICAMENTO VETERINÁRIO
Twinox 40 mg/10 mg comprimidos mastigáveis para gatos e cães
Twinox 200 mg/50 mg comprimidos mastigáveis para gatos e cães
Twinox 400 mg/100 mg comprimidos mastigáveis para cães
COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Cada comprimido mastigável contém:
Substância(s) ativa(s):
Twinox 40 mg/10 mg: Amoxicilina (sob a forma de trihidrato de amoxicilina) …40 mg; Ácido clavulânico (sob a forma de clavulanato de potássio diluído)… 10 mg
Twinox 200 mg/50 mg: Amoxicilina (sob a forma de trihidrato de amoxicilina)…200 mg; Ácido clavulânico (sob a forma de clavulanato de potássio diluído)… 50 mg
Twinox 400 mg/100 mg: Amoxicilina (sob a forma de trihidrato de amoxicilina)…400 mg; Ácido clavulânico (sob a forma de clavulanato de potássio diluído)… 100 mg
Excipiente(s): Ver Lista de Excipientes.
FORMA FARMACÊUTICA
Comprimido mastigável. Comprimidos redondos, de cor rosa, mesclados e com ranhura num dos lados. O comprimido pode ser dividido em doses iguais.
INFORMAÇÕES CLÍNICAS
Espécies-alvo
Felinos (gatos) e caninos (cães) [Twinox 40 mg/10 mg - Twinox 200 mg/50 mg].
Caninos (cães) [Twinox 400 mg/100 mg]
Indicações de utilização, especificando as espécies-alvo
Para o tratamento de infeções causadas por bactérias sensíveis à amoxicilina e ao ácido clavulânico, incluindo: infeções dérmicas (incluindo piodermite superficial e profunda); infeções dos tecidos moles (abcessos e saculite anal); infeções dentárias (por exemplo, gengivite); infeções do trato urinário; doença respiratória (envolvendo o trato respiratório superior e inferior); enterite.
Contraindicações
Não administrar em gerbilos, porquinhos-da-índia, hamsters, coelhos ou chinchilas.
Não administrar em cavalos e outros ruminantes.
Não administrar em caso de disfunção renal grave acompanhada de anúria e oligúria.
Não administrar em caso de hipersensibilidade às penicilinas ou outras substâncias do grupo β-lactâmico ou a qualquer excipiente.
Não administrar em caso de resistência conhecida à combinação de amoxicilina e ácido clavulânico.
Advertências especiais para cada espécie-alvo
Este medicamento veterinário não é indicado para casos de Pseudomonas spp.
Precauções especiais de utilização
Precauções especiais para a utilização em animais
Sempre que possível, a associação amoxicilina/ácido clavulânico deve basear-se em testes de sensibilidade. As políticas antimicrobianas oficiais nacionais e locais devem ser levadas em consideração quando o medicamento veterinário for usado. A administração do medicamento veterinário fora das instruções do RCMV pode aumentar a prevalência de bactérias resistentes à amoxicilina / ácido clavulânico e reduzir a eficácia do tratamento com outras penicilinas, devido ao potencial de resistência cruzada. Foi relatada tendência de resistência de E. coli, incluindo E. coli multirresistente.
Em animais com disfunção hepática e renal, a posologia deve ser cuidadosamente avaliada e o uso do medicamento veterinário baseado na avaliação de risco/benefício efetuada pelo médico veterinário.
Recomenda-se precaução no uso em outros pequenos herbívoros para além dos listados na seção 4.3. Os comprimidos mastigáveis são aromatizados. Para evitar ingestão acidental, guarde os comprimidos fora do alcance dos animais.
Precauções especiais a adotar pela pessoa que administra o medicamento veterinário aos animais
As penicilinas e cefalosporinas podem causar hipersensibilidade (alergia) após inalação, ingestão ou contato com a pele. A hipersensibilidade às penicilinas pode levar a reações cruzadas às cefalosporinas e vice-versa. Ocasionalmente as reações alérgicas a estas substâncias podem ser graves.
Não manusear este medicamento veterinário se souber que tem hipersensibilidade ou se tiver sido aconselhado a não trabalhar com tais preparações.
Manusear este medicamento veterinário com cuidado para evitar a exposição, tomando todas as precauções recomendadas.
Se após a exposição desenvolver sintomas, tais como erupção na pele, dirija-se imediatamente a um médico e mostre-lhe esta advertência.
Edema da face, dos lábios ou olhos ou dificuldade em respirar são sintomas mais graves e requerem atenção médica urgente.
Lavar as mãos após a administração.
Para evitar ingestão acidental, principalmente por crianças, as metades dos comprimidos não utilizadas devem ser repostas no blister aberto, este deve ser guardado na caixa e esta deve ser mantida em local seguro, fora da vista e do alcance das crianças.
Reações adversas (frequência e gravidade)
Muito raramente, podem ocorrer reações de hipersensibilidade às penicilinas em animais tratados; nestes casos, a administração do medicamento veterinário deve ser descontinuada e administrado
tratamento sintomático. Em casos muito raros, após a administração do medicamento veterinário, podem ocorrer perturbações gastrointestinais (diarreia, vómito, etc…). O tratamento pode ser descontinuado, dependendo do grau de gravidade dos efeitos indesejáveis e da avaliação de risco/benefício efetuada pelo médico veterinário.
A frequência dos eventos adversos é definida utilizando a seguinte convenção:
- muito frequente (mais de 1 em 10 animais tratados apresentando evento(s) adverso(s))
- frequente (mais de 1 mas menos de 10 animais em 100 animais tratados)
- pouco frequente (mais de 1 mas menos de 10 animais em 1.000 animais tratados)
- rara (mais de 1 mas menos de 10 animais em 10.000 animais tratados)
- muito rara (menos de 1 animal em 10.000 animais tratados, incluindo notificações isoladas).
Utilização durante a gestação, a lactação ou a postura de ovos
Os estudos de laboratório efetuados em ratos e ratinhos não revelaram quaisquer efeitos teratogénicos, fetotóxicos ou maternotóxicos. A segurança do medicamento veterinário durante a gestação e lactação não foi determinada.
Administrar a cadelas gestantes e lactantes apenas em conformidade com a avaliação benefício/risco realizada pelo médico veterinário responsável.
Interações medicamentosas e outras formas de interação
Desconhecidas.
O cloranfenicol, os macrolídeos, as sulfonamidas e as tetraciclinas podem inibir o efeito antibacteriano das penicilinas devido ao rápido início da ação bacteriostática. As penicilinas podem potenciar o efeito dos aminoglicosídeos.
Posologia e via de administração
Administração oral.
Dosagem e frequência: 10 mg de amoxicilina e 2,5 mg de ácido clavulânico / kg de peso corporal (ou seja, 12,5 mg de substâncias ativas associadas por kg de peso corporal), duas vezes ao dia (correspondendo a 25 mg de substâncias ativas combinadas por kg por dia).
A tabela a seguir destina-se a ser um guia para administrar o medicamento veterinário na dosagem recomendada:
Twinox 40 mg/10 mg
.png)
Twinox 200 mg/50 mg
.png)
Twinox 400 mg/100 mg
.png)
Para assegurar uma dose correta o peso corporal dos animais deve ser determinado tão precisamente quanto possível para evitar subdosagem.
Se o animal não aceitar o comprimido da mão ou da tigela, então o comprimido pode ser desfeito, adicionado a um pouco de alimento e dado imediatamente.
Duração do tratamento: a maioria dos casos de rotina responde a um tratamento de 5 a 7 dias. Em casos crónicos, um curso mais longo de tratamento é recomendado. Em tais circunstâncias, a duração total do tratamento deve ficar a critério do médico veterinário, mas deve ser suficiente longa para garantir a resolução completa da doença bacteriana.
Sobredosagem (sintomas, procedimentos de emergência, antídotos), se necessário
Podem ocorrer sintomas gastrointestinais ligeiros (diarreia, náuseas e vómitos) após sobredosagem do medicamento veterinário e o tratamento sintomático deve ser iniciado, quando necessário.
Intervalo(s) de segurança
Não aplicável.
PROPRIEDADES FARMACOLÓGICAS IMUNOLÓGICAS
Grupo farmacoterapêutico: Antibacterianos de uso sistémico, associações de penicilina, incluindo inibidores beta-lactâmicos.
Código ATCvet: QJ01CR02.
Propriedades farmacodinâmicas
A amoxicilina é uma aminobenzilpenicilina da família das penicilinas beta-lactâmicas. Interfere na síntese de peptidoglicano, um importante componente da parede celular bacteriana evitando, portanto,
a formação da parede celular bacteriana. O ácido clavulânico liga-se irreversivelmente à beta-lactamase e evita que a amoxicilina seja inativada.
Assim, a combinação de amoxicilina / ácido clavulânico tem um espectro notavelmente amplo de atividade bactericida contra bactérias frequentemente encontradas em cães e gatos.
A combinação in vitro de amoxicilina / ácido clavulânico é ativa contra uma ampla gama de bactérias aeróbias e anaeróbias clinicamente importantes, incluindo:
- Gram-positivos: Estafilococos (incluindo estirpes produtoras de ß-lactamase); Estreptococos.
- Gram-negativos: Escherichia coli (incluindo a maioria das estirpes produtoras de ß-lactamase) Klebsiellae; Pasteurellae.
A suscetibilidade e resistência para patógenos selecionados que causam infeções respiratórias, do trato urinário ou da pele e identificados em pesquisas europeias foram as seguintes:
Infeções respiratórias (reportadas em 2019)
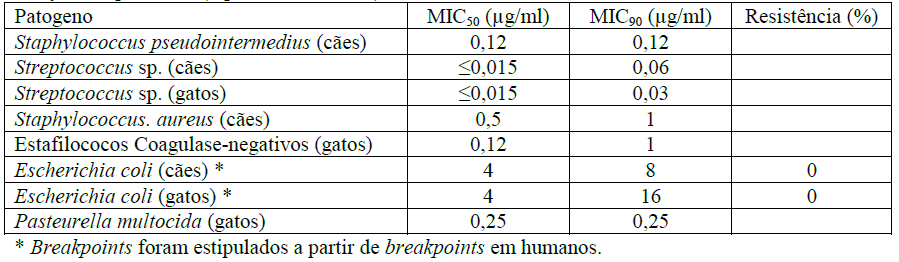
Infeções do trato urinário (reportadas em 2017 e 2019)
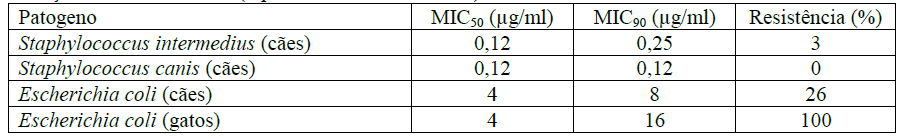
Infeções dérmicas (reportadas em 2016)
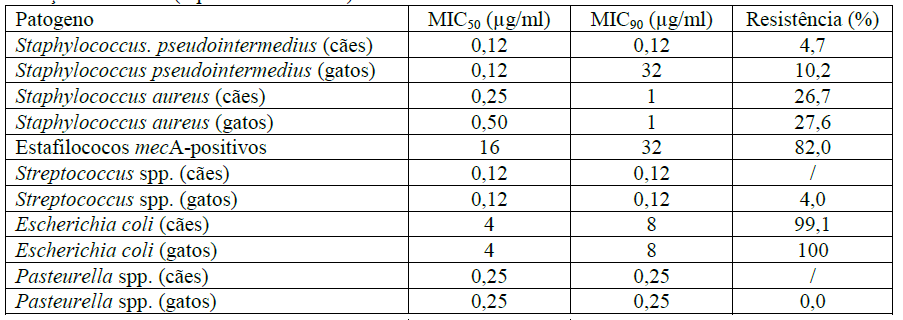
O Clinical and Laboratory Standards Institute CLSI estabeleceu os MIC breakpoint clínicos para a amoxicilina-clavulanato contra estafilococos e estreptococos que causam infeções dérmicas e dos
tecidos moles e infeções do trato urinário em gatos e cães, como ≤0.25 / 0.12 μg/ml suscetível e ≥1 /0.5 μg/ml resistente.
Para E.coli que causam infeções dérmicas e dos tecidos moles em gatos e cães, o breakpoint suscetível é estabelecido em ≤0.25 / 0.12 μg/m e para as infeções do trato urinário em ≤8 / 4 μg/ml.
Para P. multocida de origem felina, o breakpoint suscetível é estabelecido em ≤0.25 / 0.12 μg/ml e o resistente em ≥1 / 0.5 μg/ml.
Os dois principais mecanismos de resistência à amoxicilina / ácido clavulânico são:
- Inativação pelas beta-lactamases bacterianas que não são inibidas pelo ácido clavulânico, incluindo as classes B, C e D.
- Alteração das proteínas de ligação à penicilina (PLP), que reduzem a afinidade do agente antibacteriano pelo alvo (S. aureus resistente à meticilina, MRSA e S. pseudintermedius, MRSP).
A impermeabilidade das bactérias ou os mecanismos de bomba de efluxo podem causar ou contribuir para a resistência bacteriana, particularmente em bactérias Gram-negativas. Os genes de resistência
podem estar localizados em cromossomos (mecA, MRSA) ou plasmídeos (LAT, MIR, ACT, FOX, beta-lactamases da família CMY) e surgiram diversos mecanismos de resistência.
Pseudomonas aeruginosa e Enterobacter spp. podem ser consideradas como intrinsecamente resistentes à associação. A resistência é demonstrada entre Staphylococcus aureus resistente à meticilina. Tendência de resistência de E. coli é relatada, incluindo E. coli multirresistente.
Propriedades farmacocinéticas
A amoxicilina é bem absorvida após administração oral. Em cães, a biodisponibilidade sistémica é de 60-70%. A amoxicilina (pKa 2,8) tem um volume de distribuição aparente relativamente pequeno,
baixa ligação às proteínas plasmáticas (34% em cães) e uma semivida terminal curta devido à excreção tubular ativa através dos rins.
Após a absorção, as concentrações mais elevadas são encontradas nos rins (urina) e na bile e, em seguida, no fígado, pulmões, coração e baço. A distribuição de amoxicilina para o líquido cefalorraquidiano é baixa, a menos que as meninges estejam inflamadas.
Após a administração do medicamento veterinário em cães, foi alcançada uma Cmax média de 7,31 μg / ml em aproximadamente 1,37 horas. A semivida média foi de 1,21 horas.
Em gatos, foi alcançada uma média de Cmax de 5,87 μg / ml para a amocixilina em aproximadamente 1,37 horas. A semivida terminal média para a amoxicilina foi de 1,18 horas.
O ácido clavulânico (pKa 2,7) também é bem absorvido após administração oral. A penetração no líquido cefalorraquidiano é pobre. A ligação às proteínas plasmáticas é de aproximadamente 25% e a semivida de eliminação é curta. O ácido clavulânico é eliminado principalmente por excreção renal (inalterado na urina).
Após a administração do medicamento veterinário em cães, foi alcançada uma Cmax média de 1,33 μg / ml para o ácido clavulânico em aproximadamente 1,02 horas. A semivida terminal média do ácido clavulânico foi de 0,83 horas.
Em gatos, foi alcançada uma Cmax média de 3,16 μg / ml para o ácido clavulânico em aproximadamente 0,70 horas. A semivida terminal média do ácido clavulânico foi de 0,81 horas.
INFORMAÇÕES FARMACÊUTICAS
Lista de excipientes
Celulose microcristalina
Estearato de magnésio
Sílica coloidal anidra
Glicolato de amido sódico (tipo A)
Autolisado de levedura seco
Laca de alumínio eritrosina, E127
Incompatibilidades principais
Desconhecidas.
Prazo de validade
Prazo de validade do medicamento veterinário tal como embalado para venda: 2 anos.
Prazo de validade após a primeira abertura do acondicionamento primário: 24 horas.
Precauções especiais de conservação
Conservar a temperatura inferior a 25 °C.
Conservar na embalagem de origem para proteger da luz e da humidade.
Natureza e composição do acondicionamento primário
Blister formado por uma folha de alumínio que consiste numa camada de alumínio revestida com película de poliamida de um lado e PE do outro lado e uma folha de selagem de alumínio que consiste
numa camada de alumínio e revestimento de PE.
Blisters de 10 comprimidos.
Caixas de 10, 20, 100 ou 500 comprimidos.
É possível que não sejam comercializadas todas as apresentações.
Precauções especiais para a eliminação de medicamentos veterinários não utilizados ou de desperdícios derivados da utilização desses medicamentos
O medicamento veterinário não utilizado ou os seus desperdícios devem ser eliminados de acordo com os requisitos nacionais.
TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
KRKA, d.d.,
Novo mesto Šmarješka cesta 6,
8501 Novo mesto
Eslovénia
NÚMERO(S) DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
1431/01/21DFVPT - 1431/02/21DFVPT - 1431/03/21DFVPT
DATA DA PRIMEIRA AUTORIZAÇÃO/RENOVAÇÃO DA AUTORIZAÇÃO
28 de maio de 2021.
DATA DA REVISÃO DO TEXTO
Maio de 2021
PROIBIÇÃO DE VENDA, FORNECIMENTO E/OU UTILIZAÇÃO
Não aplicável.
