
Resumo de Características do Medicamento
NOME DO MEDICAMENTO VETERINÁRIO
NEOPRINIL POUR-ON 5 mg/ml solução para unção contínua para bovinos
COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
1ml de solução contém:
Substância ativa:
Eprinomectina ........................ 5,00 mg
Excipiente:
Butilhidroxitolueno (E321) ........... 0,10 mg
Todos-rac-alfa-tocoferol (E307) .... 0,06 mg.
Para a lista completa de excipientes, ver Lista de Excipientes.
FORMA FARMACÊUTICA
Solução para unção contínua.
Solução oleosa límpida, ligeiramente amarelada.
INFORMAÇÕES CLÍNICAS
Espécie(s)-alvo
Bovinos.
Indicações de utilização, especificando as espécies-alvo
Tratamento de infestações pelos parasitas sensíveis à eprinomectina, nomeadamente:
Nemátodes gastrointestinais (adultos e L4): Ostertagia ostertagi (incluindo forma larvar L4 inibida), Ostertagia lyrata (apenas adultos), Haemonchus placei, Trichostrongylus axei, Trichostrongylus colubriformis, Cooperia spp. (incluindo L4 inibida), Cooperia oncophora, Cooperia punctata, Cooperia pectinata, Cooperia surnabada, Bunostomum phlebotomum, Nematodirus helvetianus, Oesophagostomum radiatum, Oesophagostomum spp. (apenas adultos), Trichuris discolor (apenas adultos);
Parasitas pulmonares: Dictyocaulus viviparus (adultos e L4);
Larvas de mosca (fases parasitárias): Hypoderma bovis, Hypoderma lineatum;
Ácaros: Chorioptes bovis, Sarcoptes scabiei var. Bovis;
Piolhos sugadores: Linognathus vituli, Haematopinus eurysternus, Solenopotes capillatus;
Piolhos mordedores: Damalinia bovis;
Mosca dos cornos: Haematobia irritans.
O medicamento veterinário protege contra re-infestações com:
- Nematodirus helvetianus durante 14 dias.
- Trichostrongylus axei e Haemonchus placei durante 21 dias.
- Dictyocaulus viviparus, Cooperia oncophora, Cooperia punctata, Cooperia surnabada, Oesophagostomum radiatum e Ostertagia ostertagi durante 28 dias.
Contraindicações
Não usar noutras espécies que não aquelas listadas na secção 4.1 e 4.2.
Não administrar por via oral ou parenteral.
Não administrar em caso de hipersensibilidade à substância ativa ou a algum dos excipientes.
As avermectinas podem não ser bem toleradas em espécies que não são alvo (incluindo cães, gatos e cavalos). Foram relatados casos de mortalidade em cães, especialmente em Collies, Bobtail e raças relacionadas ou cruzadas e também em tartarugas.
Advertências especiais
As práticas seguintes devem ser evitadas pois aumentam o risco de aparecimento de resistências, e podem, finalmente, resultar em terapia ineficaz:
- Administração demasiado frequente e repetida de anti-helmínticos da mesma classe, durante um longo período de tempo.
- Subdosagem por subestimativa do peso corporal, má administração do medicamento veterinário, ou falta de calibração do dispositivo doseador (se existir).
Os casos suspeitos de resistência a anti-helmínticos devem ser investigados através da realização de testes adequados (ou seja, Teste de Redução de Contagem de Ovos nas Fezes). Sempre que os resultados do(s) teste(s) demonstrar(em) de forma inequívoca resistência a um determinado anti- helmíntico, deve ser administrado um anti-helmíntico pertencente a outra classe e com diferente modo de ação.
Até à data, não foi reportado na U.E. nenhum caso de resistência à eprinomectina (uma lactona macrocíclica) em bovinos. Contudo, foi reportada na U.E. resistência a outras lactonas macrocíclicas em espécies de parasitas de bovinos. Portanto, a administração deste medicamento veterinário deve basear-se na informação epidemiológica local (regional, exploração) sobre a sensibilidade dos nematodes e nas recomendações sobre como limitar ainda mais a seleção para resistência aos anti-helmínticos.
Se houver um risco de reinfeção, deve ser procurado o conselho de um médico-veterinário no que diz respeito à necessidade e frequência de administrações repetidas.
Para os melhores resultados, o medicamento veterinário deve fazer parte de um plano de controlo tanto dos parasitas internos e externos dos bovinos baseado na epidemiologia desses parasitas.
Precauções especiais de utilização
Precauções especiais para utilização em animais
Apenas para uso externo.
Para evitar os efeitos indesejáveis resultantes da destruição de larvas de mosca localizadas no esófago ou no canal vertebral, recomenda-se administrar o medicamento veterinário no fim do período de atividade da mosca e antes que as larvas possam alcançar os seus locais de repouso; consultar o médico veterinário para saber qual o período adequado para o tratamento.
O medicamento veterinário não deve ser aplicado em áreas do dorso contaminadas com lama ou fezes para não comprometer a sua atividade antiparasitária. O medicamento veterinário deve ser aplicado apenas em zonas de pele saudável.
Precauções especiais a adoptar pela pessoa que administra o medicamento aos animais
Este medicamento veterinário pode ser irritante para a pele e olhos e causar hipersensibilidade (reações alérgicas).
Evitar o contacto direto com a pele ou olhos durante o tratamento e quando cuidar de animais recentemente tratados.
As pessoas com hipersensibilidade conhecida à eprinomectina devem evitar o contacto com o medicamento veterinário.
Durante a administração do medicamento veterinário, deve ser utilizado equipamento de proteção individual e luvas de borracha.
Em caso de contacto acidental com a pele, lavar imediatamente a área afetada com água e sabão. Se a exposição acidental ocorrer nos olhos, lavar imediatamente com água.
Remover imediatamente as roupas contaminadas e lavá-las antes de voltar a usar. Este medicamento veterinário pode afectar o sistema nervoso central se ingerido acidentalmente. Evitar a ingestão acidental do medicamento veterinário, incluindo o contacto da mão com a boca. Em caso de ingestão, lavar imediatamente a boca com água e consultar um médico.
Não fumar, comer ou beber durante a administração. Lavar as mãos após a administração.
Outras precauções
A eprinomectina é muito tóxica para a fauna do estrume e para os organismos aquáticos e pode acumular-se nos sedimentos. As fezes contendo eprinomectina excretadas na pastagem por animais tratados podem reduzir a abundância de organismos que se alimentam do estrume. A seguir ao tratamento dos bovinos com o medicamento veterinário os níveis de eprinomectina que são potencialmente tóxicos para as espécies de moscas do estrume, podem ser excretados por um período superior a 4 semanas e podem reduzir a abundância das moscas do estrume durante esse período. Em caso de tratamentos repetidos com eprinomectina (ou medicamentos da mesma classe de anti- helmínticos) é aconselhável não tratar os animais sempre na mesma pastagem para permitir que a população da fauna do estrume recupere.
A eprinomectina é inerentemente tóxica para os organismos aquáticos. O medicamento veterinário só deve ser usado de acordo com as instruções do rótulo. Baseado no perfil de excreção da eprinomectina quando administrada sob uma fórmula de unção contínua, os animais tratados não devem ter acesso a cursos de água nos primeiros 7 dias após o tratamento.
Reações adversas (frequência e gravidade)
Foram observadas reações pouco frequentes como lambidelas passageiras, tremor cutâneo e seborreia e descamação no local de aplicação.
A frequência dos eventos adversos é definida aplicando a seguinte convenção:
- muito frequente (mais de 1 animal apresentando evento(s) adverso(s) em 10 animais tratados);
- frequente (mais de 1 mas menos de 10 animais em 100 animais tratados);
- pouco frequente (mais de 1 mas menos de 10 animais em 1 000 animais tratados);
- rara (mais de 1 mas menos de 10 animais em 10 000 animais tratados);
- muito rara (menos de 1 animal em 10 000 animais tratados, incluindo notificações isoladas).
Utilização durante a gestação e a lactação
Os estudos laboratoriais (rato, coelho) não revelaram quaisquer efeitos teratogénicos ou embriotóxicos quando da utilização da eprinomectina nas doses terapêuticas. Foi comprovada a segurança do medicamento veterinário em vacas gestantes e durante a lactação e em touros reprodutores. Pode ser administrado durante a gestação e lactação e em touros reprodutores.
Interações medicamentosas e outras formas de interação
O facto de a eprinomectina se ligar fortemente às proteínas plasmáticas deve ser tido em consideração quando da associação com outras moléculas com as mesmas características.
Posologia e via de administração
Uso externo. Unção contínua.
Tratamento único com aplicação tópica de uma dose de 500 μg de eprinomectina por kg peso vivo equivalente a 1ml por 10 kg de peso vivo.
O medicamento veterinário deve ser aplicado numa faixa estreita, ao longo da linha dorsal, desde o garrote até à base da cauda.
Para garantir a administração da dose correta, determinar o peso corporal da forma mais precisa possível e verificar o dispositivo doseador. No caso de tratamento coletivo, os animais devem ser agrupados de acordo com o seu peso corporal e a dose estabelecida em função deste de forma a evitar a sub e a sobredosagem.
Tratar em simultâneo todos os animais pertencentes ao mesmo grupo.
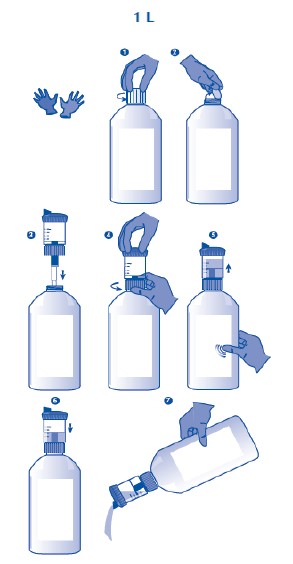
Sistema de dosificação por compressão (frasco de 1 litro)
1 e 2. Remover o selo protetor de alumínio do frasco. 3 e 4. Enroscar o copo doseador no frasco.
3 e 4. Ajustar a dose girando a parte superior do copo até alinhar o peso corporal correto com o ponteiro da tampa.
Quando o peso corporal se situar entre duas marcas, utilizar o mais alto.
5. Colocar o frasco na posição vertical e apertar até que o líquido exceda ligeiramente a linha calibrada que indica a dose requerida.
6 e 7. Ao deixar de pressionar o frasco, a dose ajusta-se automaticamente ao nível correto. Após utilização, retirar o copo doseador do frasco e enroscar a tampa no frasco.
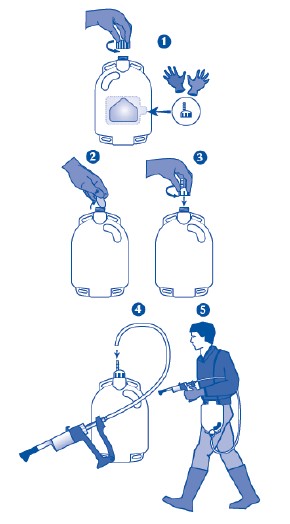
Bidão (Bidão de 2,5 litros e de 5 litros)
Adaptar a pistola doseadora apropriada e o tubo de ligação à mochila como a seguir se indica.
1 e 2. Remova o selo protetor de alumínio do frasco.
3. Substituir a tampa original do frasco pela tampa que possui o tubo de ligação.
4. Apertar a tampa de ligação. Adaptar uma extremidade do tubo à tampa de ligação e a outra extremidade à pistola doseadora.
5. Pressionar suavemente a pistola doseadora para verificar derrames.
Siga as instruções do fabricante da pistola para ajustar a dose e para o uso correto e manutenção da pistola doseadora e do tubo de ligação.
Quando o peso corporal se situar entre duas marcas, utilizar o mais alto.
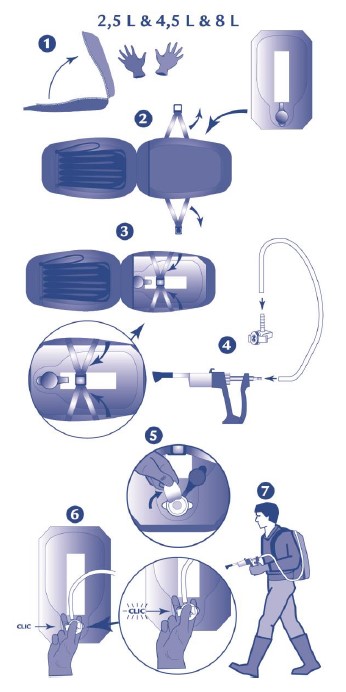
Sistema colapsável (bolsa flexível de 2,5 litros, 4,5 litros e 8 litros)
Adaptar uma pistola doseadora apropriada ao saco flexível, como a seguir se indica.
1 a 4. Adaptar uma extremidade do tubo ao sistema de acoplamento E-lock e a outra extremidade à pistola doseadora.
5 e 6. Adaptar o sistema de acoplamento E-lock ao saco flexível.
7. Pressionar suavemente a pistola doseadora para verificar derrames.
Seguir as instruções do fabricante da pistola para ajustar a dose e para o uso correto e manutenção da pistola doseadora.
Quando o peso corporal se situar entre duas marcas, utilizar o mais alto.
Sobredosagem (sintomas, procedimentos de emergência, antídotos), se necessário
Não se observaram sintomas de toxicidade após administração de até 5 vezes a dose recomendada. Não se identificou nenhum antídoto específico.
Intervalo(s) de segurança
Carne e vísceras:15 dias.
Leite: zero horas.
PROPRIEDADES FARMACOLÓGICAS
Grupo farmacoterapêutico: endectocidas, lactonas macrocíclicas, avermectinas.
Código ATCvet: QP54AA04.
Propriedades farmacodinâmicas
A eprinomectina é uma molécula com atividade endectocida, membro da classe das lactonas macrocíclicas.
Os compostos desta classe ligam-se com grande afinidade aos canais regulados por iões cloro glutamato que se encontram nas células nervosas e musculares dos invertebrados. Esta ligação seletiva destes compostos conduz a um aumento da permeabilidade da membrana celular aos iões cloro com hiperpolarização das células nervosas ou musculares, resultando na paralisia e morte do parasita.
Os compostos desta classe também podem interagir com canais de cloro regulados por outras substâncias, como os controlados pelo neurotransmissor ácido gama-aminobutírico (GABA).
Propriedades farmacocinéticas
A biodisponibilidade da eprinomectina aplicada topicamente é de cerca de 30% absorvendo-se, na sua maior parte, nos dez dias seguintes ao tratamento. A eprinomectina não é extensivamente metabolizada nos bovinos após a aplicação tópica. Em todas as matrizes biológicas, o componente B1a da eprinomectina é o resíduo simples mais abundante.
A eprinomectina contém o componente B1a (≥ 90%) e o componente B1b (≤10%) que difere numa unidade de metileno e não é extensivamente metabolizado em bovinos. Os metabolitos representam aproximadamente 10% do total de resíduos no plasma, leite, tecidos edíveis e fezes.
O perfil metabólico é qualitativa e quantitativamente muito idêntico nas matrizes biológicas referidas e não se altera significativamente algum tempo após o tratamento com eprinomectina. A relação dos dois componentes da molécula nas matrizes biológicas é idêntica à da formulação evidenciando que são metabolizados em taxas constantes aproximadas. Uma vez que o metabolismo e a distribuição tecidual dos dois componentes é similar, a sua farmacocinética deve ser também similar.
A eprinomectina liga-se intensamente às proteínas plasmáticas (99%). As fezes são a principal via de eliminação.
Impacto ambiental
Como outras lactonas macrocíclicas, a eprinomectina tem o potencial de afetar adversamente os organismos não-alvo. A excreção de níveis potencialmente tóxicos de eprinomectina pode ocorrer ao longo de um período de várias semanas após o tratamento. As fezes contendo eprinomectina excretadas no pasto pelos animais tratados podem reduzir a abundância dos microrganismos que se alimentam do estrume, o que pode ter impacto sobre a degradação do estrume.
A eprinomectina é muito tóxica para os organismos aquáticos e pode acumular-se nos sedimentos. A eprinomectina é persistente nos solos.
INFORMAÇÕES FARMACÊUTICAS
Lista de excipientes
Butilhidroxitolueno (E321)
Todos-rac-alfa-tocoferol (E-307)
Dicaprilocaprato de propilenoglicol
Incompatibilidades
Na ausência de estudos de compatibilidade o medicamento veterinário não deve ser misturado com qualquer outro medicamento veterinário.
Prazo de validade
Prazo de validade do medicamento veterinário tal como embalado para venda: 3 anos.
Prazo de validade após a primeira abertura do acondicionamento primário (frasco e bidão): 1 ano.
Prazo de validade após a primeira abertura do acondicionamento primário (sistema colapsável): 2 anos.
Precauções especiais de conservação
Este medicamento veterinário não necessita de quaisquer precauções especiais de conservação.
Natureza e composição do acondicionamento primário
Frascos HDPE branco opaco de 1 litro com selo de alumínio removível, uma tampa HDPE e um dispositivo doseador PP equipado com uma tampa dispensadora com graduações de 5 ml e volume máximo de 60 ml.
Embalagem HDPE branco opaco de 2,5 e 5 litros com selo de alumínio removível, uma tampa PP e uma tampa PP de acoplamento ventilada.
Bolsas flexíveis multicamada PET/alumínio/PA/PE de 2,5 litros, 4,5 litros e 8 litros com uma tampa PP e seu acoplamento específico POM “E-lock”.
É possível que não sejam comercializadas todas as apresentações.
Precauções especiais para a eliminação de medicamentos veterinários não utilizados ou de desperdícios derivados da utilização desses medicamentos
Extremamente perigoso para os peixes e para a vida aquática. Não contaminar lagos, cursos de água ou valas com o medicamento veterinário ou o recipiente vazio. O medicamento veterinário não utilizado ou os seus desperdícios devem ser eliminados de acordo com a legislação em vigor.
TITULAR DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
VIRBAC
1ère avenue – 2065 m – LID
06516 Carros
FRANÇA
NÚMERO (S) DA AUTORIZAÇÃO DE INTRODUÇÃO NO MERCADO
783/01/14DFVPT.
DATA DA PRIMEIRA AUTORIZAÇÃO/RENOVAÇÃO DA AUTORIZAÇÃO
2 de abril de 2014 / 14 de janeiro de 2019.
DATA DA REVISÃO DO TEXTO
Janeiro 2019.
PROIBIÇÃO DE VENDA, FORNECIMENTO E/OU UTILIZAÇÃO
Medicamento veterinário sujeito a receita médico-veterinária.
